I. EL OZONO TROPOSFÉRICO
26
Los óxidos de nitrógeno NOx
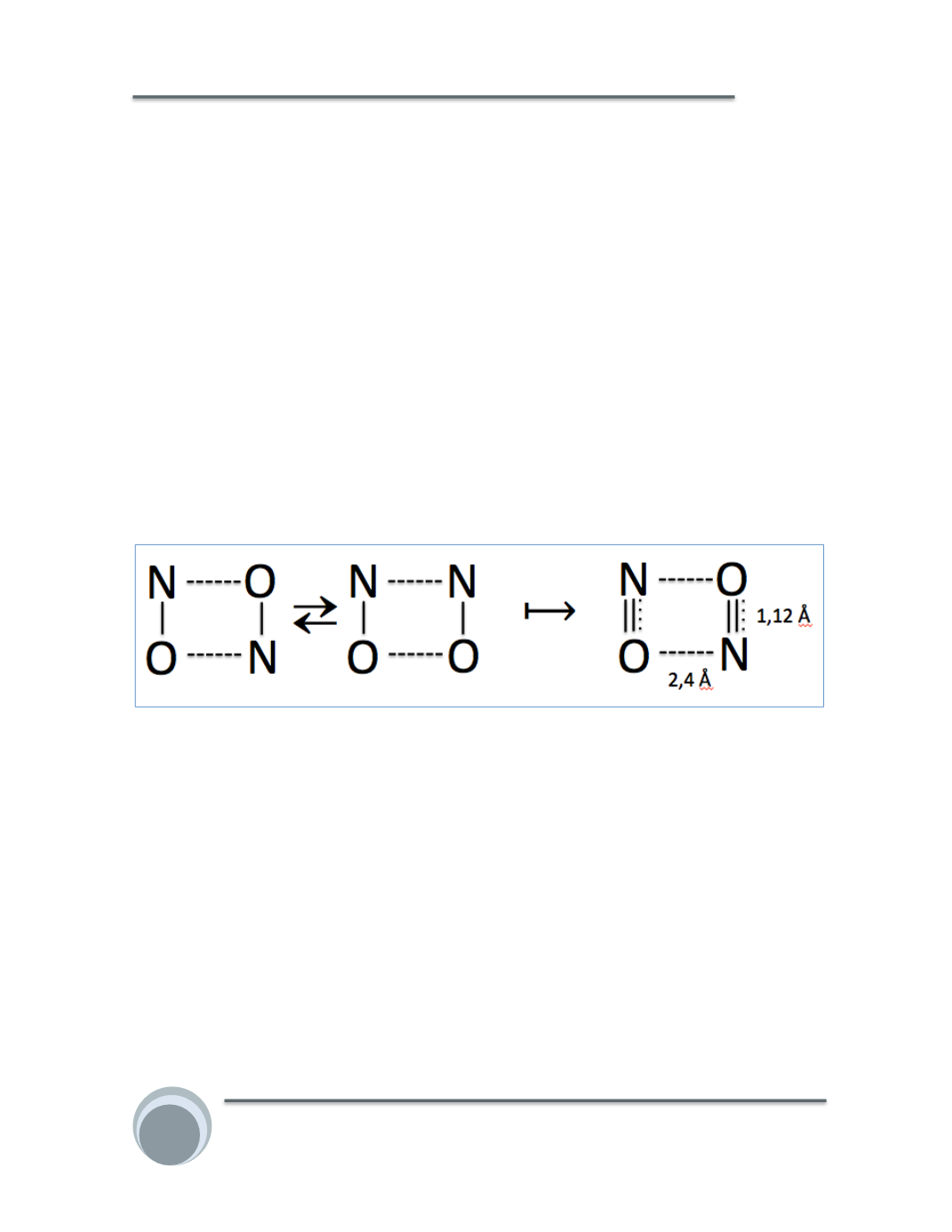
Las distancias de enlace N-‐O en el dímero (N
2
O
2
) resultan ser dos de ellas
menores (1,12 Å) que las del monómero NO (1,15 Å) y otras dos mayores (2,4 Å).
Las primeras (1,12 Å), son más cortas que las que corresponden a un doble
enlace N=O (1,15 Å), mientras que las segundas (2,4 Å) son más largas que las de un
enlace sencillo N-‐O (1,36 Å). Esas distancias N-‐O en el dímero y su diamagnetismo, son
compatibles con la presencia de atracciones electrostáticas de carga negativa entre los
átomos de N y O y el consecuente establecimiento de formas resonantes con
electrones móviles en una estructura rectangular, que representamos en la siguiente
figura:
El óxido nítrico se produce por reacción directa de nitrógeno y oxígeno:
N
2
(g) + O
2
(g)
⇄
2NO(g) ∆H = 173,4 kJ/mol
La constante de equilibrio de la reacción anterior a temperatura ambiente, es
muy pequeña (Kp=4
×
10
-‐11
a 25 °C). Por tanto, se formará muy poco óxido nítrico a
25
°
. Sin embargo, la constante de equilibrio aumenta rápidamente con la temperatura,
por lo que si se utilizan altas temperaturas se puede obtener un buen rendimiento
(22).


